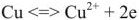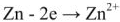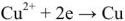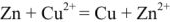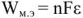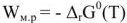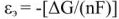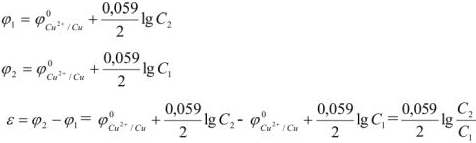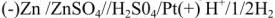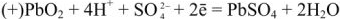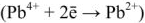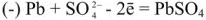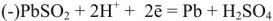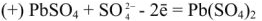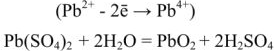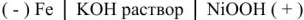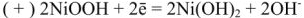- Большая Энциклопедия Нефти и Газа
- Напряжение — гальванический элемент
- ЭЛЕКТРОДВИЖУЩИЕ СИЛЫ (ЭДС) И НАПРЯЖЕНИЕ ГАЛЬВАНИЧЕСКИХ ЭЛЕМЕНТОВ
- Электродвижущая сила и напряжение гальванического элемента
- Гальванический элемент в химии
- Гальванический элемент (гэ). Напряжение гальванического элемента
- Классификация гальванических элементов
Большая Энциклопедия Нефти и Газа
Напряжение — гальванический элемент
Напряжение гальванического элемента тем выше, чем больше отличаются между собой значения стандартного потенциала электродов. [1]
Напряжение гальванического элемента может изменяться в зависимости от концентрации находящегося в нем электролита. Например, изменяя концентрацию ионов цинка в цинковом полуэлементе, мы сместим, согласно принципу Ле Ша-телье, равновесие между цинком и ионами цинка, и вследствие этого изменится электродный потенциал цинка. При [ Zn2 ] 1 моль / л стандартный потенциал этого электрода равен 0 76 В, но при уменьшении [ Zn2 ] равновесие Zn Zn2 2e — смещается в правую сторону, а поскольку электродный потенциал является мерой способности реакции к самопроизвольному протеканию, ясно, что в данной ситуации он должен возрасти. [3]
Чтобы вычислить напряжение гальванического элемента , в котором протекает заданная реакция, прежде всего представляют эту реакцию в виде двух полуреакций. [4]
Каким образом напряжение гальванического элемента связано со свободной энергией протекающей в нем реакции. Что называется стандартным потенциалом. [5]
Как вычислить напряжение гальванического элемента , если известны протекающие в нем электродные полуреакции и их потенциалы. [6]
Чему равно напряжение полученного гальванического элемента . Определите AG298 для протекающей в нем реакции. [7]
Количественной характеристикой служит напряжение гальванического элемента 0 75 В. Эта величина считается положительной, если электроны во внешней цепи двигаются от водородного к платиновому электроду. [9]
В результате измерения напряжения гальванического элемента Zn — H, изображенного на рис. 19.3, в котором [ Zn2 ] 1 М и РНг 1 атм, было установлено, что при 25 С Е 0 45 В. [10]
Потенциометрия представляет собой метод измерения напряжения гальванических элементов , составленных из двух полуэлементов, характеризующихся определенными значениями потенциалов. Один из полуэлементов должен быть стандартным электродом сравнения. [12]
Из этого выражения видно, что напряжение гальванического элемента , используемого в качеств источника тока, меньше его ЭДС. Если же уменьшать силу тока, что достигается увеличением сопротивления внешней цепи, то в пределе при бесконечно малой силе тока разность потенциалов между электродами становится равной ЭДС элемента. Но бесконечно малая сила тока означает бесконечно медленное протекание химической реакции. [13]
Из этого выражения видно, что напряжение гальванического элемента , используемого в качеств источника тока, меньше его ЭДС. Если же уменьшать силу тока, что достигается увеличением сопротивления внешней цепи, то в пределе при бесконечно малой силе тока разность потенциалов между электродами становится равной ЭДС элемента. Но бесконечно малая сила тока означает бесконечно медленное протекание химической реакции. [14]
Выбор оборудования и приборов для измерения напряжения гальванического элемента определяется требуемой точностью измерений. Для получения эталонных данных необходимо составлять цепь элемента без жидкостного соединения, измерение напряжения которого приводят с помощью прецизионных вольтметров. [15]
Источник
ЭЛЕКТРОДВИЖУЩИЕ СИЛЫ (ЭДС) И НАПРЯЖЕНИЕ ГАЛЬВАНИЧЕСКИХ ЭЛЕМЕНТОВ
Цель работы: овладение методикой измерения ЭДС и напряжения гальванических элементов
и изучение зависимости напряжения от плотности тока.
Если в гальваническом элементе протекает суммарная электродная реакция
bB + dD Û lL + mM
то ЭДС (Еэ) этого элемента записывается уравнением:

где: 




Так как активности твердых цинка и серебра принимаются равными единице, то уравнение упрощается:
Стандартную ЭДС гальванического элемента можно рассчитать либо по известным значениям стандартной энергии Гиббса реакции:
либо по разности стандартных равновесных потенциалов электродов:
Воспользовавшись вторым способом, получим:
E 
Зная стандартное значение ЭДС (потенциала) и активности ионов, можно рассчитать ЭДС
элемента (равновесный потенциал).
Если в токообразующих реакциях участвуют газообразные вещества, ЭДС элемента зависит от
парциальных давлений этих веществ. Например, ЭДС элемента, в котором протекает реакция:

где: 
Напряжение гальванического элемента меньше ЭДС из–за поляризации электродов и
где: I – ток, А; R — омическое сопротивление, Ом; ΔEЭ — поляризация элемента, равная сумме
поляризаций катода и анода, В.
С увеличением плотности тока возрастают поляризация и омическое падение напряжения. Таким образом, при увеличении плотности тока напряжение элемента падает. Кривая зависимости напряжения элемента от силы или плотности тока получила название вольтамперной кривой. По мере работы элемента (разряда) уменьшается концентрация исходных реагентов и увеличивается концентрация продуктов реакции, поэтому в соответствии с уравнением Нернста ЭДС элемента уменьшается. Кроме того возрастает поляризация элемента. Поэтому при разряде элемента напряжение его постепенно падает. Кривая изменения напряжения во времени в процессе разряда называется разрядной кривой элемента.
Опыт 1. Измерение ЭДС и напряжения элемента.
Измерение ЭДС
Гальванические элементы собирают из двух металлических электродов, помещенных в два отдельных стакана, соединенных электролитическим ключом, который представляет собой изогнутую стеклянную трубку, заполненную насыщенным раствором хлорида калия (рис. 1).
Соберите гальванический элемент, для этого подготовьте две электродные схемы, состоящие из металлов, погруженных в растворы собственных солей. Конкретные металлы – Zn и Cu.
Рисунок 1. Гальванический элемент с электролитическим ключом.
Сосуды для растворов предварительно вымойте проточной водой под краном, ополосните дистиллированной водой, затем раствором соли соответствующего металла и залейте этот раствор на 2/3 объема сосуда.
Металлические пластинки тщательно зачистите наждачной бумагой, промойте проточной водой под краном и погрузите в сосуды с раствором соли.
Проследите, чтобы места спая металлической пластины с проводником не касались раствора.
После этого подключаем гальванический элемент к высокоомному вольтметру и измеряем ЭДС. Это более простой, но менее точный метод измерения ЭДС, который заключается в прямом измерении напряжения на клеммах гальванического элемента с помощью вольтметра, имеющего высокое входное сопротивление. Вследствие высокого сопротивления мала сила тока, протекающего через элемент, поэтому невелика разница между ЭДС и напряжением элемента. Однако, даже малый ток в цепи приводит к потерям (І·R) и в результате измеряют не ЭДС, а напряжение гальванического элемента. В качестве высокоомного вольтметра в работе используется рН – метр.
1.Запишите уравнения электродных и токообразующей реакций.
2.По уравнению Нернста рассчитайте величины равновесных потенциалов электродов, использованных в элементе. Примите, что активность ионов равна концентрации.
3.Рассчитайте ЭДС и сравните ее с экспериментальным значением. Рассчитайте стандартную ЭДС элемента.
4.Используя измеренную величину ЭДС, определите энергию Гиббса токообразующей реакции и стандартную энергию Гиббса (см. Общая химия, Коровин Н.В. 2002г., стр.267). Определите стандартную энергию Гиббса по термодинамическим данным и сравните ее с расчетной.
Напряжение элемента.
Измерение напряжения проводят на установке, состоящей из амперметра для прямого измерения тока в цепи, проходящего через измеряемый элемент, вольтметра для прямого измерения напряжения на клеммах элемента и сопротивления для регулирования тока в цепи ( в отчете приведите схему установки).
Соберите гальванический элемент и подключите его к установке для измерения напряжения. Постепенно повышайте плотность тока, записывая напряжение элемента. Снимите 3-4 показания в течение 15 минут.
Результаты опыта сведите в таблицу:
Зависимость напряжения гальванического элемента от плотности тока (или тока)
| Номер измерения | Плотность тока, А/м 2 или ток, А | Напряжение элемента, В |
По данным таблицы постройте кривую зависимости напряжения элемента от плотности тока (вольтамперную кривую). Объясните, почему напряжение элемента не равно ЭДС и уменьшается при повышении плотности тока.
Источник
Электродвижущая сила и напряжение гальванического элемента
Составление схемы гальванических элементов
Для краткой характеристики гальванического элемента принято записывать его схему, в которой указываются окислители и восстановители, принимающие участие в токообразующей реакции. Первоначально указывается материал анода; затем ионы (или вещества), с которыми он находится в равновесии; затем ионы (или вещества), с которыми в равновесии находится катод и, наконец, материал катода. Граница раздела между веществами, находящимися в разных фазах (например, разных агрегатных состояниях) обозначается вертикальной чертой. Граница раздела между катодным и анодными пространством обозначается двумя вертикальными чертами. Например, схема элемента Даниэля имеет вид:
| Zn|Zn 2+ ||Cu 2+ |Cu | или | Zn|ZnSO4||CuSO4|Cu. |
Схема элемента Вольта, где катодное и анодное пространства не разделены имеет вид:
Схемы широко используются в практической электрохимии, так как являются достаточно удобными для упрощенного представления об устройстве и составе гальванических элементов.
Как было сказано выше, причиной возникновения и протекания электрического тока в гальваническом элементе является разность потенциалов электродов (DЕ). С физической точки зрения разность электродных потенциалов это — электродвижущая сила гальванического элемента (ЭДС). Поскольку в гальваническом элементе протекает самопроизвольная реакция, т.е. ток вырабатывается, то:
При этом потенциал катода больше потенциала анода (EК > EА), и в процессе работы гальванического элемента электроны перемещаются от отрицательно заряженного анода к положительно заряженному катоду. Поэтому ЭДС можно рассчитать по формуле:
При расчете ЭДС гальванического элемента, составленного из стандартных электродов в формулу (13) необходимо подставлять стандартные значения электродных потенциалов:
где DE° — стандартная ЭДС гальванического элемента.
Если же условия работы гальванического элемента отличаются от стандартных, то в формулу (13) необходимо подставлять уравнения Нернста для соответствующих полуреакций. Поэтому в общем виде, для химической реакции:
ЭДС (DE) можно рассчитать по формуле:
 | (15), |
где DE° — стандартная ЭДС; [A], [B] и [C], [D] — молярные концентрации исходных веществ и продуктов реакции соответственно; R — универсальная газовая постоянная; F — постоянная Фарадея, T — абсолютная температура, n — число электронов, принимающих участие в элементарной электрохимической реакции. Для более точных расчетов вместо молярной концентрации следует использовать значения активности ионов, принимающих участие в реакции.
При экспериментальном измерении ЭДС гальванических элементов применяются специальные методики (например, компенсационный метод) или используют измерительное оборудование, имеющее высокое внутренне сопротивление (например, высокоомные вольтметры). Чем большим сопротивлением будет обладать измерительный прибор, тем меньший ток будет протекать в цепи, тем меньшее влияние будет оказывать поляризация и тем ближе к искомой ЭДС будет показание измерительного прибора.
Реальное напряжение (U) гальванического элемента всегда меньше ЭДС из-за поляризации и омических потерь:
где I — сила тока; R — омическое сопротивление; h — поляризация элемента, равная сумме поляризаций анода и катода.
Таким образом, напряжение при разряде зависит от ЭДС элемента т.е. в основном обусловлено: типом и свойствами активных материалов электродов; составом и концентрацией электролита и деполяризатора; поляризацией; омическими потерями и температурой гальванического элемента.
По мере работы элемента (разряда) уменьшается концентрация исходных реагентов и увеличивается концентрация продуктов реакции, поэтому в соответствии с уравнением (15) ЭДС элемента уменьшается. Вследствие этого при разряде элемента напряжение его постепенно падает. С ростом же температуры напряжение гальванического элемента, как правило, немного возрастает.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Источник
Гальванический элемент в химии
Гальванический элемент (гэ). Напряжение гальванического элемента
Гальванический элемент — это, прибор, который преобразует химическую энергию окислительно-восстановительной реакции в электрическую энергию.
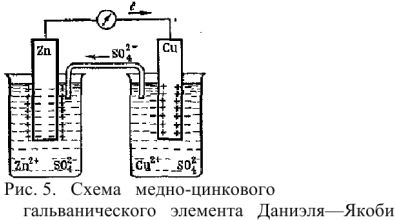
Схема простейшего ГЭ Даниэля-Якоби представлена на рис. 5.
Гальванический элемент состоит из двух электродов, каждый из которых опущен в сосуд с соответствующим раствором соли: цинковый электрод погружен в раствор соли 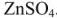
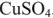
Сосуды соединены электролитическим мостиком, заполненным концентрированным раствором электролита (например, 

На поверхности цинковой пластины возникает двойной электрический слой и устанавливается равновесие
В результате протекания этого процесса возникает электродный потенциал цинка. На поверхности медной пластины также возникает двойной электрический слой и устанавливается равновесие
поэтому возникает электродный потенциал меди. Потенциал цинкового электрода имеет более отрицательное значение, чем потенциал медного электрода, поэтому при замыкании внешней цепи, т.е. при соединении цинка с медью металлическим проводником, электроны будут переходит от цинка к меди. В результате перехода электронов от цинка к меди равновесие на цинковом электроде сместиться вправо, поэтому в раствор перейдет дополнительное количество ионов цинка. В то же время равновесие на медном электроде сместиться влево и произойдет разряд ионов меди.
Итак, при работе элемента Даниэля-Якоби протекают следующие процессы:
1) реакция окисления цинка
Процессы окисления в электрохимии получили название анодных процессов, а электроды, на которых идут процессы окисления, называют анодами;
2) реакция восстановления ионов меди
Процессы восстановления в электрохимии получили название электродных процессов, а электроды, на которых идут процессы восстановления, назвают катодами;
3) движение электронов во внешней цепи;
4) движение ионов в растворе: через электролитический мостик анионов 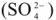
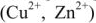
Вследствие этой химической реакции в гальваническом элементе возникает движение электронов во внешней цепи и ионов внутри элемента, т.е. электрический ток, поэтому суммарная химическая реакция, протекающая в гальваническом элементе, называется токообразующей.
При схематической записи, заменяющей рисунок гальванического элемента, границу раздела между проводником 1-го рода и проводником 2-го рода обозначают одной вертикальной чертой, а границу раздела между проводниками 2-го рода — двумя чертами. Схема элемента Даниэля-Якоби, например, записывается в виде:
для упрощения в таких схемах обычно опускается внешняя цепь. Как видно, в гальваническом элементе идет химическая реакция, а во внешней цепи элемента протекает электрический ток, т.е. в гальваническом элементе происходит превращение химической энергии в электрическую.
Электродвижущая сила. Напряжение элемента. Электрическая работа равна произведению разности потенциалов электродов на количество электричества. Максимальная разность потенциалов электродов, которая может быть получена при работе гальванического элемента, называется электродвижущей силон (ЭДС) элемента. Она равна разности равновесных потенциалов катода и анода элемента.
= 
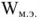
где 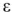
В то же время максимальная полезная работа 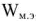
Так как 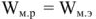
Значения термодинамических характеристик процесса получаются равными 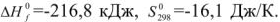
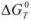
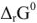
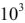
Согласно уравнения Нернста один и тот же электрод при различных концентрациях ионов имеет различное значение потенциала, поэтому возможны так называемые концентрационные ГЭ. Рассмотрим, например, ГЭ, составленный из двух медных электродов, опущенных в электролиты с разными концентрациями ионов 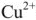
Положим, что 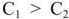
Работа в концентрационном ГЭ совершается не за счет реакции окисления восстановления, а за счет выравнивания концентрации растворов. Если концентрация электролитов отличаются в 10 раз, то напряжение (э.д.с.) ГЭ равна 0,0295 в, а если в 100 раз, то — 0,059 в.
Применяются для определения одной из концентраций 
Концентрационная и химическая поляризация электронов.
На медном катоде в замкнутом элементе происходит восстановление ионов меди. При этом концентрация их при электродном слое снижается и тем сильнее, чем больше сила тока. Это затрудняет протекание реакции восстановления, и скорость катодной реакции определяется скоростью диффузии ионов к электроду. Уменьшение концентрации катионов меди по формуле Нернста приводит к уменьшению величины потенциала меди. Цинковый анод растворяется и тем с большей скоростью, чем больше сила тока. Это приводит к накоплению ионов цинка в приэлектродном слое, в результате чего его потенциал смещается по указанной причине в положительную сторону. Электроды в этом случае поляризуются благодаря изменению концентрации ионов у их поверхности. Такая поляризация носит название концентрационный или диффузионный.
В ряде случаев кроме поляризации, при протекании тока имеет место и так называемая химическая поляризация. Для иллюстрации этого явления составим следующую цепь:
В данном случае на платине восстанавливаются не ее ионы, поскольку их нет в растворе, а ионы водорода до атомного водорода, который адсорбируется на платине и частично растворяется в ней, а также превращается в молекулярный водород. Платиновый электрод, таким образом, превратится в водородный, т.е. изменится химическая природа электрода. При этом его потенциал сместится в отрицательную сторону. Иными словами, произойдет химическая поляризация катода, которая, как и концентрационная, приводит к уменьшению напряжения гальванического элемента.
Классификация гальванических элементов
Гальванический элемент состоит из двух электродов: катода (+) и анода (-) и из одного или дух электролитов, разделенных между собой пористой перегородкой, ограничивающей их смешивание. Известны типы гальванических элементов: химические, концентрационные,
окислительно-восстановительные. В гальваническую пару можно сочетать также электроды, принадлежащие к различным видам. При таком сочетании электродов не представляется возможным классифицировать элементы, исходя из природы электродов. Классификация окажется очень громоздкой. Поэтому элементы подразделяют по другим признакам: по особенностям работы, назначению и конструкциям.
Гальванические элементы делят на первичные химические источники тока и вторичные. К первичным относятся вес ранее рассмотренные элементы. Их можно использовать только один раз. После разряда они становятся непригодными к дальнейшей работе.
К вторичным относят аккумуляторы (накопители электричества). Аккумулятор после разряда можно снова зарядить, г.е. превратить продукты реакции путем электролиза в исходные вещества. При этом электрическая энергия превращается в химическую.
Первичные источники тока в свою очередь делят на элементы с жидким электролитом (наливные) и «сухие» (непроливающиеся) элементы с загущенным электролитом. Сухие элементы можно подразделить по признаку катодных деполяризаторов на элементы с твердыми окислителями, воздушной системы и смешанной марганцово-воздушной системы.
Аккумуляторы. Аккумуляторы — обратимые гальванические элементы.
Вещества, из которых изготовляют электроды, и электролиты подобраны в аккумуляторах с таким расчетом, чтобы обратимость химических процессов при электролизе (зарядке) достигалась с минимальной потерей энергии на побочные реакции и в виде теплоты.
Понятно, что медно-цинковый элемент с двумя разделенными пористой перегородкой растворами не пригоден в качестве аккумулятора. Так как происходящие в нем диффузионные процессы необратимы. При этом восстановление ионов цинка до металлического при зарядке будет сопровождаться побочной реакцией восстановления водорода.
Из огромного количества исследованных гальванических элементов удовлетворяют указанным требованиям свинцовый аккумулятор Плантэ, железо-никелевый (кадмиево-никелевый) аккумулятор Эдиссона и серебряно-цинковый аккумулятор Андре.
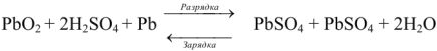
Свинцовый аккумулятор (рис. 6) был изобретен в результате работ Якоби, Плате и братьев Тюдор. В незаряженном виде он состоит из свинцовых пластин, отлитых в виде решеток. Отверстия отрицательных решеток заполнены пастой из свинцового глета РЬО и воды, а положительных — суриком 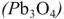

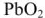
Перед использованием в аккумулятор наливают 30%-ый раствор серной кислоты.
При этом образуется гальваническая цепь:
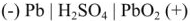
При разрядке аккумулятора на электродах протекают следующие реакции: на катоде
на аноде
Вещества катода и анода превращаются в сернокислый свинец, а химическая энергия — в электрическую.
При зарядке аккумулятора на электродах протекают следующие реакции:
на катоде
на аноде
Суммируя процессы зарядки и разрядки, получим:
В гальваническом элементе катод заряжен положительно, а анод -отрицательно. При электролизе, наоборот, катод заряжен отрицательно, а анод -положительно. Однако в любом случае на катоде протекает реакция восстановления, а на аноде — окисления. При зарядке и разрядке аккумулятора полярность электродов остается неизменной.
Исходя из равновесных потенциалов 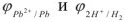
После того как на катоде закончится восстановление катионов свинца до металлического свинца, а на аноде — окисление 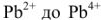
Емкость свинцового аккумулятора около 35вт/ч (20000 кулонов) на 1 кг веса. Последняя возрастает с повышением концентрации кислоты до некоторого предела; максимум емкости соответствует концентрации кислоты около 30% (плотность 1,224).
Свинцовый аккумулятор отдает около 80% подведенной к нему электроэнергии и дает примерно 4 а/ч на 1 дм2 поверхности пластин. Аккумулятор считают практически разряженным, если его напряжение на зажимах упало на 10% (от 2 в).
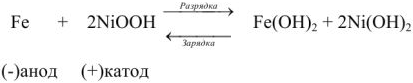
В щелочном аккумуляторе Эдиссона электродами служат порошкообразное железо и (гидрат окиси никеля, который частично дегидратируется до 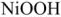
К электролиту часто добавляют гидрат окиси лития 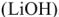
Электроды щелочных аккумуляторов изготавливают в виде пакетов из стальной стали с большим числом отверстий для прохода электролита к действующей массе, закладываемой в пакеты. При сборке пластины изолируют одну от другой эбонитовыми стержнями.
При разрядке на электродах протекают следующие процессы:
на катоде
на аноде
Напряжение щелочного аккумулятора равна 1,33 — 1,40 в.
При зарядке на катоде железо из гидрата закиси восстанавливается до металлического; на аноде 
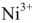
Суммарно процесс зарядки и разрядки можно изобразить следующим уравнением:
Максимальное напряжение при зарядке щелочного аккумулятора равно 1,8 в, конечное напряжение при разрядке 1 — 1,1 в. К.п.д. у щелочных аккумуляторов меньше, чем у свинцовых. Преимуществом щелочных аккумуляторов является их малый вес, простота ухода за ними, а также то обстоятельство, что случайные короткие замыкания не приносят такого вреда, как свинцовым аккумуляторам. При большой скорости образования сернокислого свинца он полу рыхлым, в результате чего электроды аккумулятора разрушаются.
Срок службы щелочных аккумуляторов в зависимости от электролита составляет 250-750 циклов.
Эта теория взята со страницы помощи по химии:
Возможно эти страницы вам помогут:





















































Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института
Источник